En båtägares guide till korrosion
Denna guide är avsedd att ge dig en grundläggande förståelse för vad korrosion är, vad som orsakar och påverkar den, och hjälpa dig att avgöra vilket anodmaterial som är rätt för din båt.
Av alla de komplicerade ämnen en båtägare behöver känna till är korrosion förmodligen det mest förvirrande. Korrosion kan orsaka konsekvenser för både båtunderhåll och båtsäkerhet. Vissa typer av korrosion kan till och med devalvera din investering på några månader eller till och med dagar.
Vad är korrosion?
Korrosion är en elektrokemisk process som orsakar försämring av metallkomponenter när de utsätts för en fuktig/våt miljö, såsom vatten. Detta sker både under vattnet och i atmosfären.
Försämring är den process där metallen förändras till sin oxidform. Stål, till exempel, kommer att brytas ned (oxideras) tillbaka till sitt naturliga stabila tillstånd, nämligen rost.
Korrosionsprocess
Metallatomerna vid ytan avger elektroner och omvandlas till positivt laddade joner, som löses upp i vattnet eller elektrolyten (en vätska som kan leda elektricitet). Elektroner strömmar genom metallen från korrosionsområdet till andra områden i närheten, där de bildar negativa joner i vattnet. De positiva jonerna strömmar genom vattnet och kombineras med de negativa jonerna som strömmar i motsatt riktning.
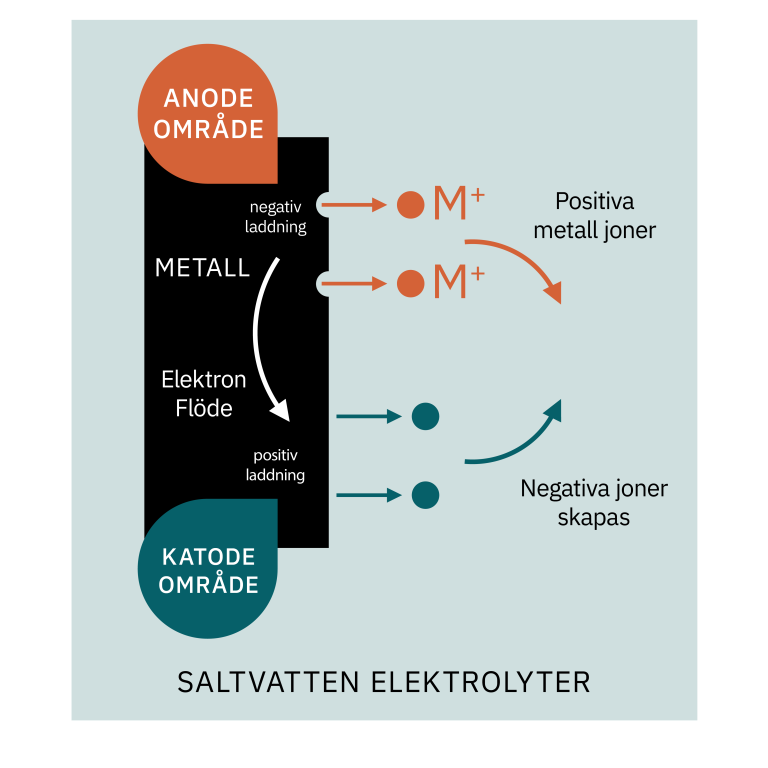
Så du kan se att en elektrisk ström skapas mellan två områden på metallytan, vilket resulterar i metallförlust (korrosion) vid de områden som agerar anod. Endast elektroner avges vid katodområdena, så ingen metall går förlorad i dessa områden. De är faktiskt skyddade.
Galvanisk korrosion
När två olika metaller (koppar och stål i exemplet) är i kontakt kommer elektroner att flöda från den mer negativt laddade metallen (anod) till den mer positiva metallen (katoden). Spänningen som genereras mellan koppar och stål skulle vara 0,3 volt. Kretsen fullbordas av förlusten av positivt laddade joner, från anoden in i elektrolyten, och de negativt laddade jonerna vid katoden.
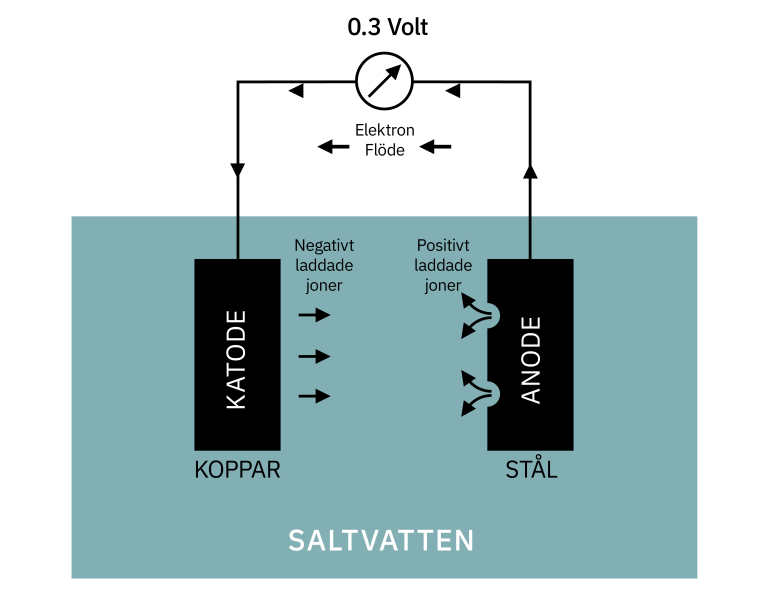
Illustration av en galvanisk korrosion
Detta utsläpp av små partiklar (joner) i vattnet är mycket snabbare än med en ensam metall och är begränsad till stålets korrosion. Katodmaterialet (koppar) är skyddat.
Offeranod
Om du vill skydda båda typerna av metall måste du ha en tredje mer aktiv metall. Den vanligaste metallen är zink, även om magnesium och aluminium också används. Denna aktiva metall blir anoden för båda metallerna.
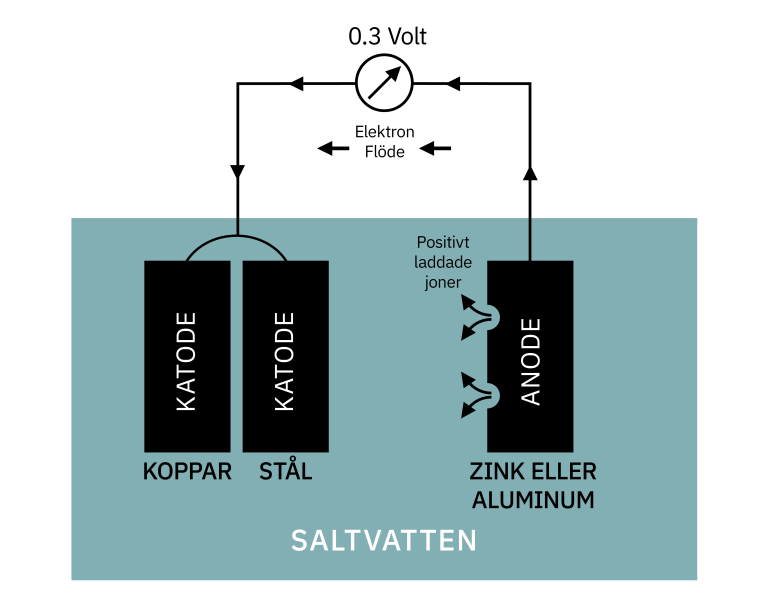
Illustration av offeranod
Zinken eller aluminiumet offrar sig för att skydda de andra två metallerna, därav termen offeranod.
Varför korroderar vissa metaller mer än andra?
Alla metaller tenderar att oxideras (korrodera), vissa lättare än andra. Här kan man lista en del av den galvaniska ordningen:
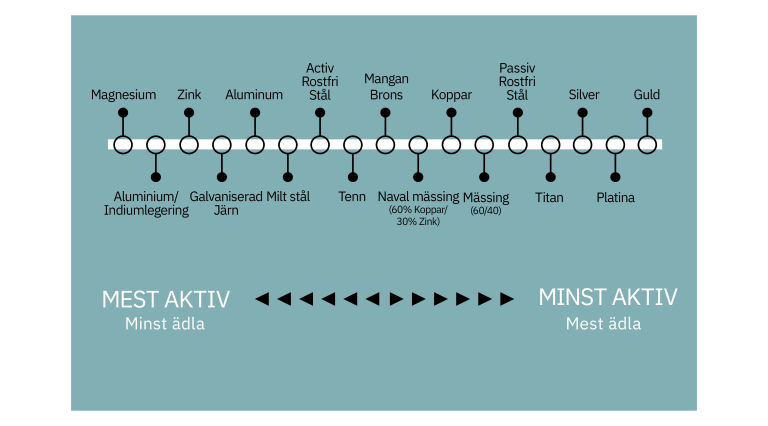
Illustration av en galvanisk ordning
Vilka faktorer påverkar korrosion?
Var medveten om att vissa av dessa faktorer kan variera mikroskopiskt på metallytan.
- Elektrolytens ledningsförmåga - havsvatten är en bra ledare och sötvatten en dålig ledare, så korrosion är värre i havsvatten.
- Mängd syre - i allmänhet ökar korrosionshastigheten i proportion till mängden syre i vattnet. Men sprickor och sprickor, som är områden som svälter på syre, blir anodiska och korroderar också.
- Förekomst av föroreningar - ökar korrosion.
- Flödeshastighet - ökar korrosionshastigheten. Gropbildning i rostfritt stål minskar dock.
- Temperatur - högre temperatur ökar korrosionshastigheten, ungefär fördubblas för varje 10°C/18°F
- Spänning - metall under dragpåkänning (sträckt) i kombination med korrosion kan drabbas av plötsligt brott på grund av spänningssprickor.
- Förekomst av bioorganismer - det finns olika typer av mikroorganismer som kan bidra till korrosion, antingen genom att ta bort skyddet eller orsaka en frätande miljö.
Yta och vikt på anod
Ytan på offeranoderna avgör hur mycket skydd (amperage) du får. Vikten avgör hur länge de håller. Olika anoder har olika kapacitet mätt i amperetimmar per pound.
Katod till anod förhållande
Förhållandet mellan det katodiska (skyddade) området och den anodiska (korroderande) ytan är avgörande vid galvanisk korrosion. Ju mindre område där anoden avger material, desto snabbare kommer det att ske. Helst bör det anodiska området vara mycket större än det katodiska området. Detta förhållande kan förbättras genom att måla den katodiska ytan.
Galvanisk korrosion via jordledningen
Anslutning till landström ansluter din jord till närliggande båtar. Om lämpliga anoder inte skyddar dessa båtar, kommer du att vara den som skyddar dem – vilket orsakar snabb slitage på dina anoder. Se diagrammet nedan:
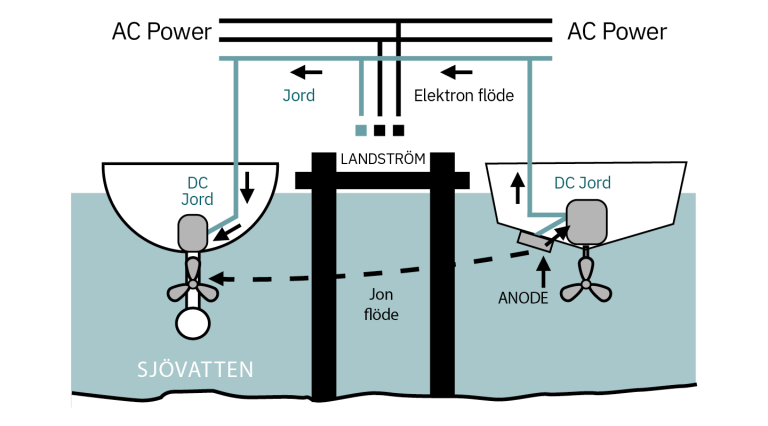
Illustration av korrosion via landström jord
Galvanisk isolator
En galvanisk isolator är en enhet som är installerad på jordledningen för att blockera direkta galvaniska strömmar men ändå låta AC passera. Se upp: Se till att din galvaniska isolator är klassad för den effekt du använder, t.ex. 30A eller 50A. Galvaniska isolatorer av dålig kvalitet har varit kända för att starta bränder, så det är en bra idé att skaffa en som är ABYC-godkänd eller UL-listad för att säkerställa att den har testats ordentligt.
Krypström (elektrolytisk) korrosion
Denna korrosion orsakas av en extern ström som flyter från ett batteri eller annan likströmskälla. Denna ström rinner ut ur metallen i vattnet och orsakar förlust av material eller korrosion i processen. Vanliga orsaker är en blottad ledning i länsen på felaktigt ansluten eller installerad utrustning.
Zinksaver system
Istället för att använda en offeranod för att generera en skyddsspänning kan en likströmskälla användas. Principen är densamma, men strömmen övervakas och justeras av ett system. Ett icke-korroderande material används för anoden.
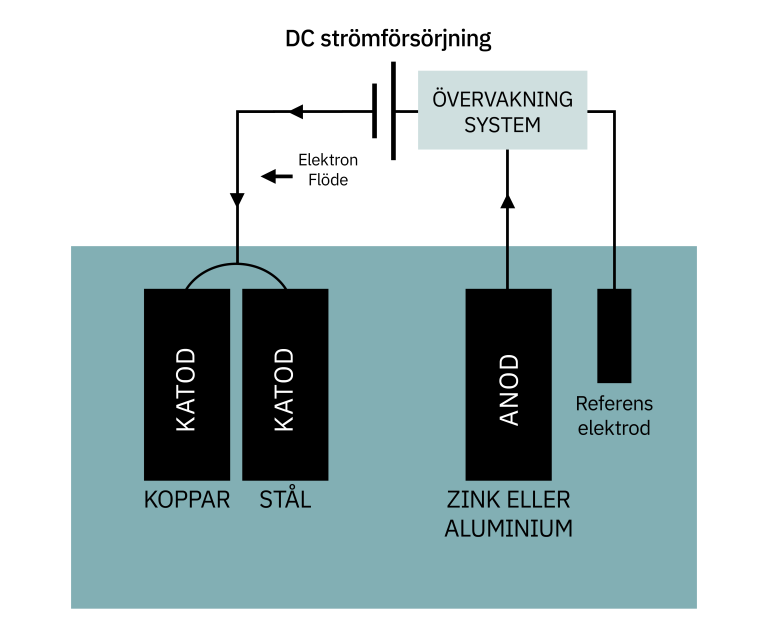
Illustration med zinksaver system
Fördelen med ett zinksaver system är att det kan utveckla högre spänningar än en offeranod. Nackdelen är att den kan "överskydda".
Koppling
All elektrisk utrustning och metall under vatten ska anslutas till samma jordpunkt (ansluten till batteriets minuspol). Detta säkerställer att alla komponenter har samma spänning, vilket förhindrar att eventuella krypströmmar uppstår.
Offeranodmaterial

Zink anoder
Zink är det vanligaste materialet som används. Zinkanoder är inte särskilt användbara i sötvatten och kan sluta fungera efter bara några månader om de inte görs enligt millimeterspecifikationer. Det är en bra policy att byta dem regelbundet, även om de ser ok ut. Kom ihåg att om en anod inte slits bort så fungerar den inte!
Aluminum anoder
Den aluminiumlegering som används i anoder skiljer sig mycket från vanlig aluminium. Den innehåller cirka 5 procent zink och ett spår av indium, vilket förhindrar att ett oxidskikt byggs upp. Aluminiumanodlegering ger mer skydd och håller längre än zink (se diagram). Det kommer att fortsätta att fungera i sötvatten och är säkert att använda i saltvatten. Aluminium är den enda anoden som är säker för alla användningsområden.
Magnesium anoder
Magnesium är den mest aktiva metallen på galvanisk skala. Den kan användas i sötvatten, men försiktighet måste iakttas. Magnesium kan överskydda aluminiumskrov eller drev i salt- eller bräckt vatten eller till och med förorenat sötvatten, vilket gör att ytbehandlingen lyfts med resulterande korrosion. Även några timmars nedsänkning kan orsaka allvarlig skada.
Vilket anodmaterial är rätt för din båt?
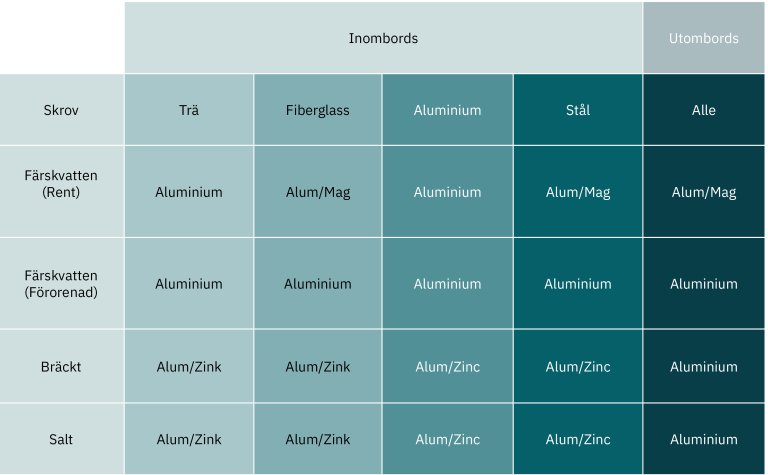
Anod vad du bör och inte bör göra
Bör göra
- Byt dina anoder när de är 50 procent korroderade. en "slitageindikator" anod hjälper dig att tala om när du ska byta.
Se till att de har god elektrisk kontakt - ta bort färg och rengör monteringsytan.
Skydda trimplan individuellt (limma inte). Även om de vanligtvis är gjorda av rostfritt stål kan de fortfarande korrodera och behöver offeranoder.
På drev, se till att använda nya skruvar/bultar (som vanligtvis levereras med anoden) - även rostfria bultar går sönder på grund av korrosion.
Håll ett drev nedsänkt i vattnet så att anoderna kan fungera.
Bör inte göra
- Måla inte anoder. De kommer inte att fungera!
- Blanda inte anodtyper - aluminiumanoder försöker skydda zinkanoder på samma bindningskrets.
- Använd inte zinkanoder på drev i aluminium - de ger då inte rätt skydd.
- Använd inte magnesiumanoder på drev i salt- eller bräckt vatten eftersom de kommer att "överskydda" aluminiumet.
Snabb fakta om marina material
Aluminum
Rätt vald aluminiumlegering är ett utmärkt material för marint bruk. Metallen väger lite, är stark och lätt att arbeta med. Dessutom har aluminium i allmänhet utmärkt korrosionsbeständighet på grund av dess förmåga att snabbt bilda en skyddande oxidationsfilm på sin yta. Oskyddad kan den utsättas för lokal korrosion, även kallad gropkorrosion, där området täcks av ett grovt vitt pulver. Denna form av korrosion är vanlig för alla metaller som bildar oxidskikt, men dessa är oftast ytliga och inte skadliga. Anodisering kommer normalt att eliminera detta.
Samtidigt är aluminium mycket aktivt på den galvaniska skalan (-,76- 1,00 volt), vilket gör det benäget för galvanisk korrosion vid kontakt med ädlare metaller. Beslag av brons, mässing eller monel bör undvikas eller isoleras för att förhindra galvanisk korrosion. Rostfria fästanordningar (316) rekommenderas. Aluminium kan överskyddas av för hög spänning från magnesiumanoder i saltvatten, bräckt vatten eller förorenat sötvatten.
Mässing
Mässing är en legering av koppar och zink. Generellt sett rekommenderas inte för maritimt bruk. Mässing är benäget att avzinka, vilket är den galvaniska korrosionen av zink från legeringen, vilket gör att mässingskomponenterna blir porösa. Men det finns avzinkningsbeständiga mässing som rekommenderas för marina miljöer. Observera att manganbrons är mässing, inte en äkta brons, och behöver galvaniskt skydd om den används under vatten.
Brons
Brons är en legering av koppar med lite eller ingen zink. Autentisk brons är robust och extremt motståndskraftig mot korrosion, både i atmosfären och i vatten. Brons kan innehålla tenn, aluminium, nickel eller fosfor, men det bästa och mest använda är kiselbrons. Används i delar som kommer att vara i en maritim miljö och/eller nedsänkta i vatten under lång tid.
Rostfritt stål
Rostfritt stål är ett mycket använt, korrosionsbeständigt material. Rostfritt har sin korrosionsbeständighet på grund av sin kromhalt som bildar en oxidfilm som tätar ytan mot angrepp av korrosion (materialet kallas då passivt).
Om rostfritt stål isoleras så att nytt syre inte når ytan, till exempel under tätningar eller rör, tappar det sin skyddande oxidfilm och blir aktivt. Det kommer då lätt att korrodera. Detta kan även uppstå i mikroskopiska sprickor som resulterar i nästan osynlig korrosion, vilket kan orsaka plötsliga skador som att propelleraxlar går sönder utan förvarning. Som ett exempel kan korrosion inuti propelleraxellagren också orsakas av denna brist på syre i området och det resulterande nedbrytningen eller hindrandet av det rostfria materialets förmåga att bygga upp en skyddande oxidfilm på ytan som ett resultat.
Trä skrov
Träskrov är mycket känsliga för nedbrytning på grund av olika träslag och korrosion orsakad av metallbeslag och fästelement. Silikonbronsfästen rekommenderas.
Glasfiber/kompositskrov
Med glasfiber- och/eller kompositskrov rekommenderas bronsfästen under vattenlinjen. Varning: Kolfiber (grafit) är elektriskt ledande och kan orsaka galvanisk korrosion mellan metallkomponenter i strukturen.
Användbara länkar
- The truth about aluminum anodes - by Martin Wigg and Paul Fleury (pdf)
- Basics of corrosion - by Performance Metals (pdf)
- Sacrificial anodes FAQ - by Performance Metals (pdf)
Referens: Performance Metals

